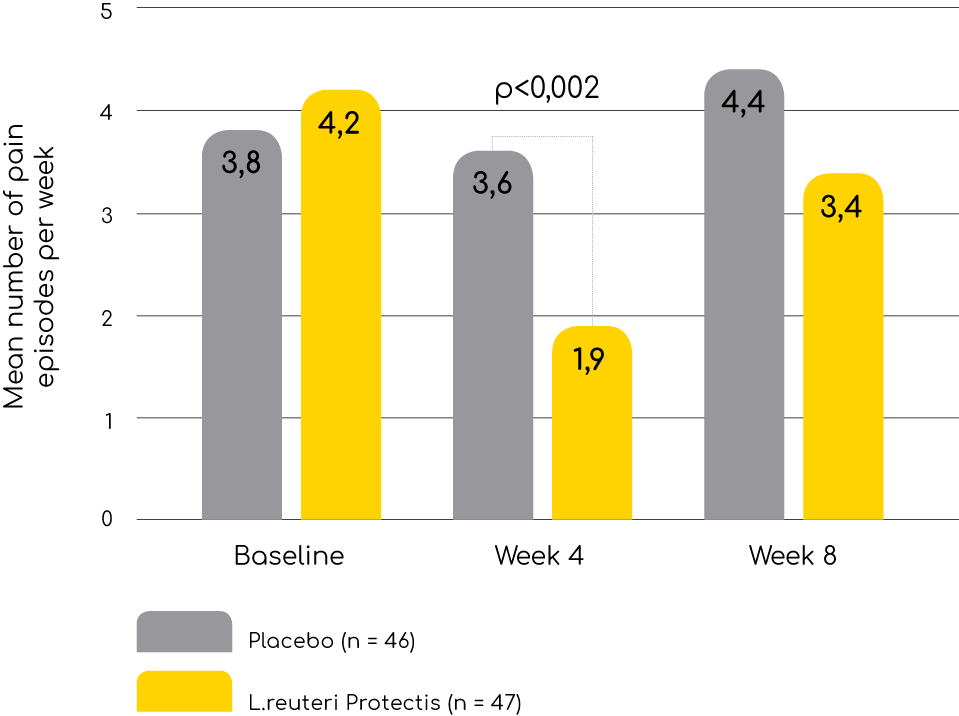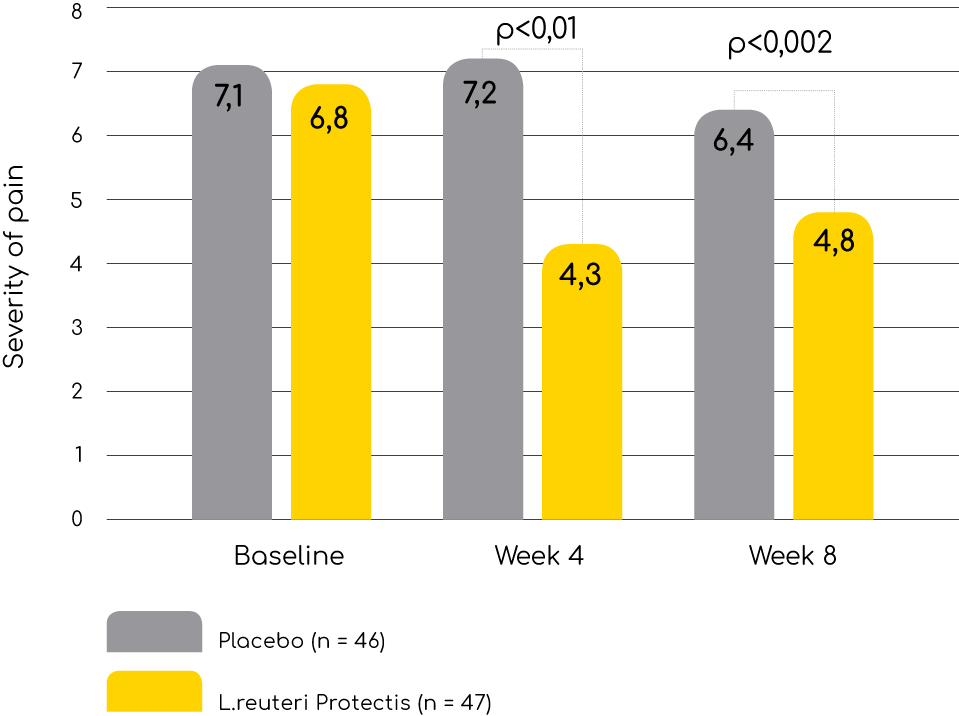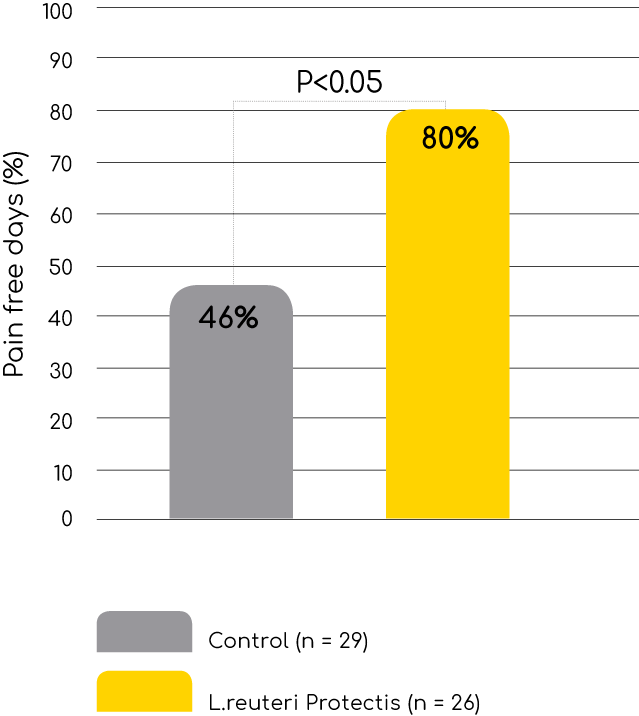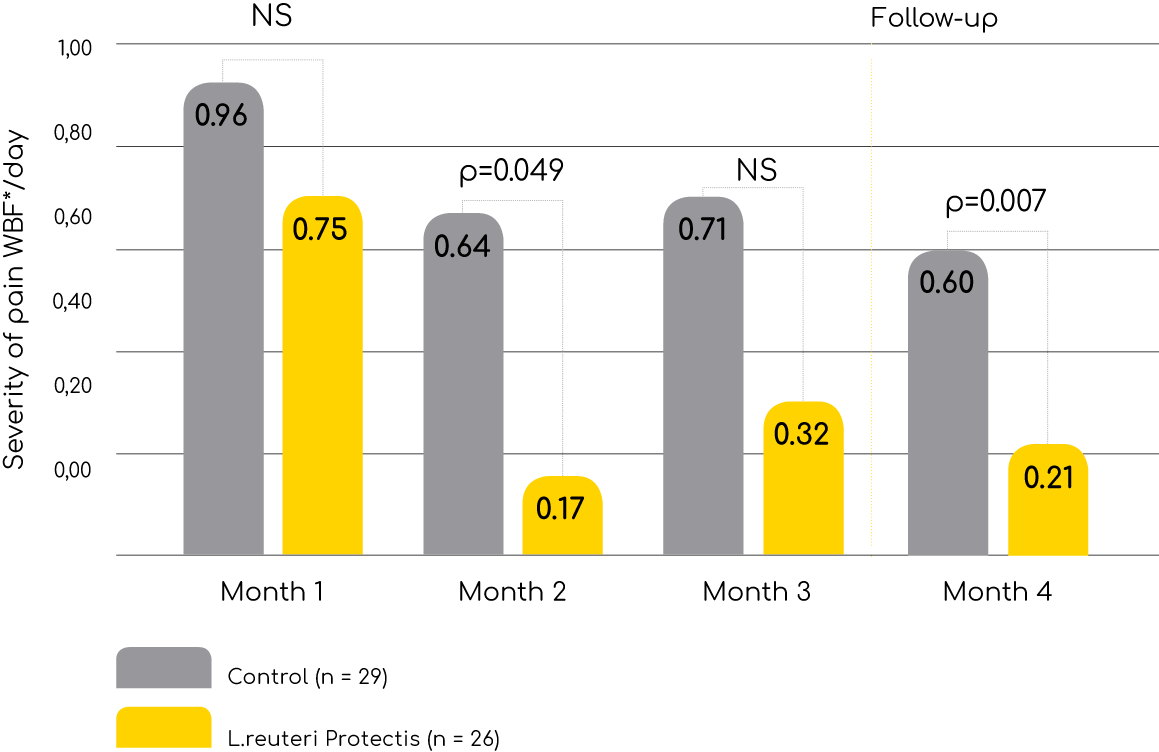
Ból brzucha o charakterze czynnościowym (FAP)
Ból brzucha czynnościowy (FAP) dotyka do jednej piątej wszystkich dzieci w wieku szkolnym i jest jednym z najczęściej diagnozowanych problemów medycznych w dziedzinie pediatrii. Jednak przyczyny tego schorzenia są nadal niejasne.